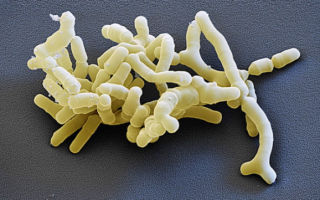
Люди думают, что они хозяева своей жизни. Но самонадеянные Homo sapiens ошибаются. Нашей жизнью управляют триллионы крошечных существ. Они не умеют ни думать, ни говорить, но это совершенно не мешает им принимать за нас решения.
Если взять условного среднего Homo sapiens — 30 лет, ростом 170 см и весом 70 кг — и посчитать, сколько в нем клеток, то получится примерно 30 триллионов (триллион — это единица и 12 нулей). Бактерий в таком усредненном человеке окажется примерно столько же.Крошечные существа живут у нас повсюду: на лбу, в подмышках, в носу и во рту, на пятках, половых органах и подушечках пальцев. Микробиолог Роб Найт и его коллеги из Колорадского университета в Боулдере выяснили, например, что бактерии, населяющие правую руку, отличаются от тех, что обитают на левой. Более того, на каждом пальце процветает особое микробное сообщество, непохожее на сообщества на других пальцах. Анализируя бактерий, живущих на компьютерной мыши, можно с вероятностью 90% выяснить, чья она.Но больше всего микробов обитает в кишечнике. Бактерии заполняют все его отделы, помогают нам усваивать пищу и синтезировать некоторые витамины. Долгое время считалось, что этим роль кишечных обитателей и ограничивается, поэтому ученые и врачи уделяли им не слишком много внимания. Однако в последние годы стало очевидно, что люди здорово недооценивали своих «соседей». За миллионы лет совместной жизни обитающие в наших внутренностях микробы научились отлично управлять высокомерным «транспортом». Их цель — жить максимально комфортно, размножаться и получать вдоволь пищи. Чтобы добиться этого, бактерии заставляют нас делать то, что нужно им, причем мы даже не замечаем, что нами руководят.
Настроение: работа «кишечного мозга»
У каждого бывали дни и месяцы, когда настроение портится без видимой причины. А потом вдруг налаживается — опять как бы само по себе. Последние научные данные указывают, что необъяснимыми перепадами настроения могут «дирижировать» живущие в кишечнике бактерии. Многие из них умеют синтезировать «человеческие» нейромедиаторы — вещества, которые управляют работой мозга.
Например, 90% серотонина — нейромедиатора, дающего нам хорошее настроение и спокойствие, — производится именно кишечными бактериями. Микробы синтезируют и многие другие важнейшие вещества, в том числе главное успокоительное нервной системы гамма-аминомасляную кислоту (ГАМК) и основной нейромедиатор мотивации дофамин.Кишечных бактерий исследуют, получая материал из прямой кишкиДобраться до мозга кишечные нейромедиаторы не могут — их не пропускает так называемый гематоэнцефалический барьер, плотный слой клеток, фильтрующий потенциально опасные вещества. Но воздействовать на голову, чтобы изменить настроение, необязательно: в наших внутренностях есть собственный «мозг», с которым и работают бактерии. Разные отделы кишечника усеяны более чем 100 миллионами нейронов — это намного больше, чем, скажем, в спинном мозге. «Кишечный мозг» не умеет решать уравнения или запоминать иностранные слова, зато он 24 часа в сутки следит за процессами, которые протекают в наших внутренностях, и «подкручивает» их в зависимости от условий. Часть информации отправляется по так называемому блуждающему нерву наверх — «главному мозгу», и, влияя на эту информацию, бактерии могут контролировать наше настроение.В 2011 году исследователи из канадского Университета Макмастера и Ирландского национального университета в Корке кормили лабораторных мышей лактобактериями Lactobacillus rhamnosus. Животные, которые регулярно съедали несколько миллиардов этих микробов, становились заметно более спокойными и меньше реагировали на стрессовые воздействия — из-за того что в их мозгу изменялся синтез рецепторов к ГАМК. Но если мышам перерезали блуждающий нерв, эффект пропадал. Ученые полагают, что L. rhamnosus и другие микробы каким-то образом воздействуют на «кишечный мозг» и блуждающий нерв, а уже он передает в головной мозг сигнал, что необходимо изменить синтез тех или иных молекул.
Депрессия и стресс: заразная грусть
Склонностью к определенному поведению можно «заражать» других при помощи нужных микробов. Ирландские ученые выделили бактерий, обитающих в кишечнике людей с клинической депрессией, и пересадили их крысам, которых вырастили в стерильных условиях, то есть своего микробиома у них не было.
Очень быстро здоровые до этого крысы потеряли интерес к жизни, начали отказываться от еды и проводить почти все время в уединенных укрытиях. Изменился и метаболизм их нейромедиаторов: по всем признакам у животных развилась депрессия.Бактерии Verrucomicrobia найдены в водоемах и кишечнике людейТочно так же можно «заражать» грызунов любовью осваивать все новое. После пересадки бактерий от мышей-исследователей равнодушные к приключениям стерильные сородичи тоже начинали активно изучать вольеры и лабиринты.Кстати, сами по себе стерильные мыши всегда отличаются повышенной тревожностью. И это неспроста. Когда животное появляется на свет, в норме его внутренности немедленно заселяют бактерии: сначала из родовых путей матери, потом из окружающей среды. «Въехав» в новый дом, микробы начинают подавать различные химические сигналы, которые корректируют работу физиологических систем ответа на стресс. И если вовремя не «снабдить» животных бактериями, они развиваются неадекватно чувствительными. Поэтому так важно обеспечивать приток «правильной» флоры грудничкам, особенно если они родились путем кесарева сечения и не получили маминых бактерий. Излишняя стерильность в этом деле только навредит.Бактерии группы Bacteroides — главная «массовка» кишечника. Они же вызывают множество опасных болезнейПСИХОФИЗИОЛОГИЯНевидимая рукаВопрос, способны ли бактерии при помощи каких-то химических сигналов заставлять своих хозяев есть определенные продукты, остается открытым. Но косвенные данные указывают, что это хотя бы отчасти возможно: когда человек поглощает «неправильную» с точки зрения населяющих его кишечник бактерий пищу, она переваривается медленно, вызывая дискомфорт.
По блуждающему нерву эта информация от «нижнего» мозга может передаваться «верхнему», и человек, сам не понимая почему, решает больше не есть эти продукты.
Ожирение: голодные гены«Заражать» можно не только депрессией и склонностью к исследованиям, но и… ожирением. Стерильные мыши, которым пересаживали бактерий из кишечника людей с лишним весом, за несколько недель толстели в два раза. Животные, получившие микробов от худых Homo sapiens, оставались стройными. Но и это еще не все. Ученые из Университета Эмори работали с мышами, имеющими мутацию в гене TLR5, — животные и люди с таким генетическим дефектом все время голодны и из-за этого переедают. Когда исследователи подсадили бактерий из кишечника мутантных мышей здоровым грызунам, те немедленно начали есть все подряд и быстро растолстели. Но когда специалисты при помощи антибиотиков уничтожили микрофлору животных с мутацией TLR5, звери прекратили набрасываться на съестное и их вес нормализовался.Сообщество микробов ротовой полости обширно и разнообразноКак именно бактерии заставляют животных переедать, пока неясно, но, похоже, микробы и метаболизм работают сообща. В кишечнике полных людей формируется сообщество микробов, которые любят поесть, и они при помощи разных механизмов заставляют хозяина все время перекусывать. При этом неважно, связана ли изначальная причина ожирения с генетикой или же лишний вес стал следствием распущенности: после того как внутри обосновались «толстые» бактерии, человек превращается в обжору в любом случае. Хорошая новость в том, что, убив «неправильных соседей», можно восстановить нормальный метаболизм. Впрочем, вместе с гадкими бактериями легко уничтожить и полезных, поэтому не стоит бездумно принимать антибиотики: шансов, что вы навредите себе, а не поможете, куда больше.
Иммунитет: прояснение этиологии
Микробиом крайне важен для нашей иммунной системы. Лакто- и бифидобактерии ослабляют воспалительные процессы, в том числе хронические, которые способствуют развитию сердечно-сосудистых заболеваний. Как именно микробы воздействуют на иммунитет, до конца неясно.
Похоже, что выделяемые бактериями вещества, в том числе короткоцепочечные жирные кислоты (КЖК), влияют на работу генов иммунной системы. Когда ученые «заставляли» кишечных бактерий производить больше КЖК, у животных утихали симптомы аллергии, которая, казалось бы, никак с кишечником не связана.Бифидобактерии создают в кишечнике благоприятные условия для других «хороших» микробовАллергия не единственный пример. Жировое перерождение печени, легочные заболевания, атеросклероз, предшественник диабета метаболический синдром, многие виды рака и другие болезни, которые считались «бесхозными», то есть возникающими по неясным причинам, оказались связаны с нашими одноклеточными сожителями. Но не в том смысле, что те или иные микробы вызывают какой-то недуг: бактериальная регуляция иммунитета куда тоньше и изощреннее. По мере роста в организме формируется сообщество «своих» бактерий, которые не вызывают иммунного ответа и помогают ему лучше работать. Более того, эти микробы отчасти формируют саму иммунную систему: у стерильных мышей ее клетки отличаются от иммунных клеток обычных мышей и по внешнему виду, и по активности. Если нормальное «общение» между микробиомом и хозяином почему-либо нарушается, хозяин начинает болеть. Ученые обнаружили у животных целый ряд специальных структур, которые распознают всевозможные выделяемые бактериями вещества и корректируют работу организма, руководствуясь полученной информацией.
- МЕНЮ
- Вегетарианское здоровье
Разные типы бактерий извлекают энергию из разных источников, и еда, которая подходит одним микробам, бесполезна или ядовита для других. Люди, которые едят много сладкого и жирного, «выращивают» у себя в кишечнике микробов, умеющих перерабатывать именно такие продукты. Микроорганизмы, получающие энергию из условного творога, во внутренностях сладкоежек попросту не выживают. Радикально отличаются по составу микробиомы вегетарианцев и мясоедов. В кишечнике первых преобладают бактерии групп Prevotella и Bacteroidetes, а внутренности вторых населены микробами Bacteroides и Firmicutes. Микрофлора тех, кто ест мало животного белка, заметно многообразнее, и в ней реже встречаются патогенные энтеробактерии. Ученые из Италии и Ирландии показали, что обилие «мясных» бактерий связано с повышенным риском атеросклероза и диабета второго типа.
Такие бактерии выделяют опасные вещества, например триметиламиноксид, провоцирующий в том числе накопление бляшек в сосудах. Есть данные, что у обладателей большого количества «вредных» бактерий иначе работают гены, вовлеченные в развитие диабета и сердечно-сосудистых заболеваний. Ученые полагают, что на их работу тоже влияют выделяемые микробами соединения.
Хочу конфетку, хочу грустить: как кишечные бактерии управляют нашими желаниями
Триллионы микробов живут в каждом взрослом человеке, и это нормально. Часть из них помогает нам жить, запуская биохимические реакции, другая часть тащит нас по врачам. Целый зоопарк обитает в кишечнике: сотни видов бактерий, вирусов и грибков.
Именно их называют кишечным микробиомом, или кишечной микрофлорой. Большинство обитает в «кармане» толстой кишки — так называемой слепой кишке.
Некоторые специалисты даже считают микробиом полноценным органом человеческого тела, настолько слаженно работают его компоненты.
Микробиом, или микрофлора кишечника, — это все микробы в кишечнике, которые действуют как еще один орган, имеющий решающее значение для вашего здоровья.
Откуда же берутся эти микробы? Изначально у новорожденного нет микробиома, но с молоком матери он наследует от нее первые бактерии, которые обживаются на новой территории.
С этого момента начинается «сотрудничество» человека со своим микробиомом.
Пока человек обеспечивает бактериям питание (всё, что попадает в кишечник, — это их шведский стол), они взамен помогают на всех фронтах: переваривают пищу, производят полезные питательные вещества, гормоны и даже формируют иммунитет.
Но есть и бактерии с «темной стороны»: они вызывают не только проблемы с пищеварением, но и провоцируют развитие сердечно-сосудистых заболеваний и других проблем — от аллергии до деменции. И представьте: эти коварные враги виноваты даже в вашем обжорстве (хотя нет, не только они).
Ваш мозг захвачен
Ах да, микробы влияют и на поведение человека-хозяина. И на самом деле эффективная связь между мозгом и кишечником налажена давно. Например, кишечные бактерии производят в организме около 95% серотонина — «гормона счастья». Микробы могут таким образом поднять настроение человеку, а могут испортить. Доказано и влияние некоторых кишечных микробов на развитие депрессии.
Удивительно, но еще древние греки предполагали, что психические расстройства возникают, когда пищеварительный тракт производит слишком много черной желчи. Как недалеки они были от истины!
Но как же микробы это делают? Науке пока известно три основных механизма воздействия кишечной микрофлоры на мозг человека:
- Производство нейрохимических веществ (тот же серотонин), которые мозг использует для регуляции не только физиологических процессов, но и психических, таких как обучение, память, изменение настроения. Эти вещества, в основном гормоны, из кишечника проникают в кровеносные сосуды и напрямую попадают в мозг.
- Микробы воздействуют на нейропод — специальные клетки слизистой оболочки кишечника, которые могут стимулировать соседние нервные клетки, в том числе блуждающий нерв, напрямую соединенный с мозгом.
- Воздействие через иммунные клетки. Так уж сложилось, что в человеческом кишечнике находится примерно 70% всего иммунитета. Микробы живут по соседству с иммунными клетками, работают вместе с ними и регулярно их «пинают»: заставляют реагировать, воспроизводить армию себе подобных, если в организме есть опасность, и т. д. В итоге от микрофлоры многое зависит: какие антитела и в каком количестве направятся по кровотоку к месту воспаления или в мозг.
«Это не ты хочешь чизбургер, это твои бактерии хотят чизбургер»: как общение бактерий и их разборки влияют на поведение человека
Как именно происходит воздействие на иммунные клетки, нетрудно догадаться: кишечные бактерии только и делают, что выделяют разные вещества, а те в свою очередь влияют на процессы в вашем «богатом внутреннем мире».
И с иммунными клетками точно такая же история. Например, стенка бактерии производит вещество, которое стимулирует иммунные Т-клетки вырабатывать белки, регулирующие сон человека.
А те продлевают активную фазу сна или же вызывают бессонницу у пожилых людей.
Когда микробы хотят сладкого
И вот сенсация для любителей перевести стрелки: это не вы хотите сладкого, а микробы внутри вас. Оказывается, жители кишечника регулярно влияют на наш выбор питания.
Такое открытие помогли сделать мухи. Так уж вышло, что для начальных исследований эти насекомые просто идеальны, так как их кишечная микрофлора содержит лишь несколько видов организмов.
Португальских ученых озадачила стая голодных мух, которые избегали дрожжей, хотя любят этот продукт из-за содержащегося в нем ценного белка. Но странные особи подлетали к пище и заворачивали крошечные носики вверх, не принимая угощение.
Как связаны эмоции и ЖКТ
Биологи обнаружили, что в организме этих мух есть определенные микробы, меняющие их аппетит и пристрастия к еде.
В ряде исследований отмечено, что бактерии могли сами производить недостающие компоненты белка, а заодно «сообщать» организму мухи, что без дополнительного белка он и так проживет. Именно поэтому мухи игнорировали дрожжи. В других исследованиях отмечены микроорганизмы, для которых эти белки губительны, поэтому микробам было выгодно управлять мухой, запрещая ей лакомиться дрожжами.
Опыты на мышах подтвердили эту взаимосвязь. Обычно мыши благоразумно убегают, когда чувствуют запах кошачьей мочи. Но существует микроорганизм-паразит, называемый токсоплазмой. Мышей, зараженных им, привлекает кошачья моча. Они жаждут ее и идут на запах, становясь обедом для кошки.
В основном исследования проводились на животных, но были опыты и на людях. И, например, выяснилось, что люди, которым хотелось шоколада, имели в моче микробные метаболиты, отличные от тех, что были у испытуемых, к шоколаду безразличных, несмотря на идентичную в обеих группах диету.
Зачем микробам ваше ожирение?
Мотив коварных микроорганизмов понятен: в кишечном зоопарке разные виды бактерий конкурируют друг с другом за жилплощадь. Здесь каждый заинтересован в том, чтобы по пищеводу спустился именно его вид пищи. Одним для выживания нужно острое, другим — жирное и сладкое, а третьим, напротив, — поменьше сладкого и побольше клетчатки из овощей.
Микробы могут повлиять на наш выбор питания разными путями: вызвать тягу к пище, на которой они специализируются, или же к продуктам, подавляющим их конкурентов — полезные бактерии.
А могут провоцировать болезненные ощущения до тех пор, пока мы не съедим пищу, которая им необходима. Так что если вы ощущаете, что мозг настойчиво требует сладкого, возможно, это вовсе не ваш организм.
Просто он в заложниках, а требования диктует микроскопический террорист.
Как с этим жить?
Кто же победит — болезнетворные микробы или полезные? Здесь, как и в старой притче, побеждает тот волк, которого вы кормите.
Всего лишь изменив рацион, можно уменьшить популяцию болезнетворных микробов и помочь полезным бактериям жить и размножаться.
Например, диета с неперевариваемыми углеводами — цельнозерновыми и пшеничными отрубями — увеличивает количество кишечных бифидобактерий и лактобацилл, которые участвуют в синтезе ценных аминокислот, защитных механизмах и переваривании пищи.
В то же время эксперименты на мышах показали уменьшение количества бифидобактерий при диете с высоким содержанием жиров.
Хорошая новость: микробов много, но живут они недолго и очень зависимы от питания, которое мы им предоставим.
Если микробиом новорожденного полностью зависит от микробиома и рациона кормящей матери, а также окружающей среды, то микробиом взрослого во многом в его собственных руках.
Специалисты из Гарвардской школы медицины рекомендуют есть больше ферментированных продуктов, клетчатки и сложных углеводов для заселения кишечника полезными микробами. И важно: питание должно быть разнообразным.
Когда в кишечнике живут микроорганизмы «разных национальностей», возникает здоровая конкуренция, где право на выживание есть у каждого.
В противном случае некоторые микробы становятся монополистами: легко подавляют жизнь конкурентов, а в свободное от их уничтожения время посылают в мозг человека «заявки» на вредные деликатесы.
Другой вариант — прием аптечных препаратов, пребиотиков. Но и тут не стоит ждать чуда: их общая эффективность до конца не исследована, да и эффект недолговечен. Пребиотики — это препараты на основе микробов.
Их задача — восполнять полезные бактерии, убитые антибиотиками. Это не означает заселить кишечник бактериями, словно Марс — колонизаторами.
Бактерии из препарата лишь создают условия, которые мешают росту болезнетворных микробов и помогают восстанавливать популяцию полезных.
Медики даже рассматривают как вариант лечения заболеваний пересадку кала от здорового человека к больному. Да, кала.
Трансплантация фекалий здорового донора человеку с кишечным колитом, например, или стройного человека пациенту с ожирением — это лечение, основанное примерно на том же принципе, что и лечение пребиотиками. Нужно пересадить часть здорового микробиома, содержащегося в каловой массе, чтобы создать конкуренцию болезнетворным микробам.
Сейчас ученые активно изучают эффективность такого метода при лечении самых разных заболеваний — от воспаления кишечника до аутизма. И уже есть результаты. Несколько исследований на мышах показали, что трансплантация фекалий между тучными и худыми животными может изменять их метаболизм, по сути, делая толстых мышей худыми и наоборот.
А вот испытаний на людях было немного. Да и результаты довольно противоречивы. В первом подобном опыте 22 тучных, но в остальном относительно здоровых взрослых человека в течение 12 недель принимали капсулы с препаратом. У одной половины испытуемых капсулы содержали образцы кала здоровых худощавых людей, а другая половина принимала плацебо.
В итоге микробиом людей, принимавших реальный препарат, и правда изменился, став похожим по составу на кишечную микрофлору доноров. Однако исследователи пытались выяснить, изменяет ли фекальный трансплантат концентрацию гормона, участвующего в насыщении.
И, к сожалению, через 12 недель никаких изменений в уровне этого гормона не зарегистрировали, как не заметили и изменения массы тела испытуемых.
В любом случае одного исследования недостаточно, чтобы делать однозначные сенсационные выводы. Однако для микробиологов исследования кишечного зоопарка — очень перспективная тема.
И пока одни люди под контролем микробов опустошают холодильник и витрины кондитерских лавок, другие используют это явление в своих интересах. Например, разрабатывают бактериальные препараты для лечения психических расстройств.
Впрочем, не исключено, что это одни и те же люди.
В одном ученые пока уверены: чтобы жить долго и счастливо, стоит дружить со своим «богатым внутренним миром». Кстати: бактериальных клеток в теле человека больше, чем его собственных. Так что мы их хозяева или они — наши? Вот вам отличная тема для вечеринки философов.
Как микробиота борется со стрессом и депрессией
Никого не удивит, что дисбактериоз или нарушение баланса микробиоты влияет на настроение: сложно быть бодрым и веселым, испытывая проблемы с пищеварением и дискомфорт. Но ученые доказали, что кроме настроения активность кишечных бактерий влияет на уровень тревожности и восприимчивость к стрессу. А сбалансированная микрофлора помогает психике с этим справляться.
Содержание
Связь кишечника и мозга
Кишечник с мозгом соединяет блуждающий нерв, основной элемент вегетативной нервной системы, которая регулирует работу внутренних органов. Благодаря этой системе мы дышим, глотаем и перевариваем пищу не задумываясь.
Блуждающий нерв помогает перемещать пищу по желудочно-кишечному тракту, стимулирует производство пищеварительных ферментов и позволяет понять, насколько мы сыты.
А еще этот нерв помогает мозгу следить за тем, все ли в порядке с кишечником.
Стресс, микробиота и депрессия
Стресс вызывет выброс гормона кортизола и увеличивает проницаемость кишечника. Из-за этого эндотоксины, которые образуются при распаде бактерий, могут попасть в кровь и вызвать иммунную реакцию. Начинается воспаление, а нервная система реагирует на него в том числе изменением настроения. Так могут появиться симптомы депрессии и тревожности.
Ученые обнаружили, что постоянное воспаление часто сопутствует депрессии и тревожности, а прием противовоспалительных снимает эти симптомы.
Кроме того, психическое состояние влияет на состав микробиоты и может вызвать дисбактериоз. Например, исследования показывают, что у пациентов с депрессией становится значительно больше бактерий из родов Bacteroidetes, Protobacteria и Actinobacteria, а вот представителей рода Faecalibacterium у них наоборот мало, и чем меньше, тем серьезнее симптомы.
Дисбактериоз в свою очередь, ослабляет защитную функцию слизистой кишечника и провоцирует воспаление. А это только усугубляет психическое состояние.
Диета против депрессии и тревожности
Восстановить баланс микробиоты и вернуть хорошее настроение можно, если подкорректировать диету. Про- и пребиотики помогают восстановить соотношение видов бактерий и снизить проницаемость слизистой кишечника. Исследования показывают, что такие продукты улучшают реакцию организма на стресс и уменьшают воспаление, а уровень тревожности и симптомы депрессии уменьшаются вместе с ним.
Ешьте больше растительной пищи
Полезные кишечные бактерии любят натуральную, растительную пищу, где много клетчатки.
Когда вы едите пребиотики: фрукты и овощи, орехи, цельнозерновые продукты или бобовые, бактерии вырабатывают масляную кислоту.
Это незаменимая короткоцепочечная жирная кислота, которая поддерживает здоровье кишечника. Она помогает предотвратить воспаление, а значит избежать проблем с пищеварением и сохранить хорошее настроение.
Список продуктов, богатых пребиотиками:
| Чеснок | Бобовые | Лук |
| Лук | Семена | Яблоки |
| Ягоды | Зерновые | Чай |
| Топинамбур | Охлажденный после приготовления картофель | Какао |
| Грибы | Зеленые бананы | Красное вино |
| Рожь | Плантан (овощной банан) | Красные фруткы |
| Ячмень | Кукуруза | Соевые бобы |
Добавьте в рацион пробиотики
Пробиотики поддерживают здоровый баланс микробиоты и предотвращают дисбактериоз. Исследования показывают, что определенные штаммы лактобацилл повышают устойчивость к стрессу и тревоге, а еще прием пробиотиков может облегчить симптомы депрессии.
На заметку:
Кишечник и мозг тесно взаимосвязаны и влияют друг на друга. Стресс и дисбактериоз ухудшают настроение и влияют на риск развития тревожности и депрессии. А депрессия в то же время может нарушить баланс микробиоты и привести к развитию воспаления.
Рацион, богатый про- и пребиотиками, помогает снять воспаление, восстановить баланс микробиоты, повысить устойчивость к стрессу и ослабить депрессию и тревогу.
С Тестом Микробиоты Атлас вы сможете узнать, в порядке ли баланс ваших бактерий и что стоит добавить в рацион, чтобы лучше справляться со стрессом.
- Ansari, F et al. The Effects of Probiotics and Prebiotics on Mental Disorders: A Review on Depression, Anxiety, Alzheimer, and Autism Spectrum Disorders, 2020
- Benakis, C et al. The Microbiome-Gut-Brain Axis in Acute and Chronic Brain Diseases, 2020* Cheung, S, G et al. Systematic Review of Gut Microbiota and Major Depression, 2019* Liu, H et al. Butyrate: A Double-Edged Sword for Health? , 2018
- Liu, L and Zhu, G. Gut-Brain Axis and Mood Disorder, 2018
- Peirce, J, M and Alviña, K. The Role of Inflammation and the Gut Microbiome in Depression and Anxiety, 2018
- Stakenborg, N et al. The Versatile Role of the Vagus Nerve in the Gastrointestinal Tract, 2014
- Winter, G et al. Gut Microbiome and Depression: What We Know and What We Need to Know, 2018
- de Punder, K., & Pruimboom, L. Stress induces endotoxemia and low‐grade inflammation by increasing barrier permeability. 2015
- Müller, N. et al. The cyclooxygenase‐2 in‐ hibitor celecoxib has therapeutic effects in major depression: Results of a double‐blind, randomized, placebo controlled, add‐on pilot study to reboxetine.2006
до -65%
Генетический тест
до -65%
29 900 ₽
С Новым годом!
Генетический тест со скидкой до 65%
С Новым годом!
Тест микробиоты со скидкой до 25%
Новогодняя распродажа
до -65%
Генетический тест
Новогодняя распродажа
до -25%
Тест микробиоты
Бактерии помогают производить "гормон счастья" в кишечнике
Хотя серотонин и известен как нейромедиатор мозга, по оценкам, около 90% от его общего количества в организме производится в желудочно-кишечном тракте. Иногда в простонародии серотонин называют «гормоном счастья» или хорошего настроения, но на самом деле это очень узкое представление о роли данного соединения в организме человека…
Изменения уровней этого так называемого периферийного серотонина связаны с различными заболеваниями, в том числе с синдромом раздражённого кишечника (СРК), сердечно-сосудистыми заболеваниями и остеопорозом.
Новое исследование специалистов из Калифорнийского технологического института показало, что некоторые бактерии кишечника имеют большое значение для производства периферического серотонина.
«Всё больше и больше исследований показывают, что мыши и другие модельные организмы демонстрируют изменения в поведении в ответ на изменения в микробном составе их кишечников, – рассказывает Элейн Сяо (Elaine Hsiao), профессор биологии и биоинженерии и ведущий автор исследования. — Мы заинтересованы проследить взаимосвязь микробов и нервной системы. Для начала мы изучили, как кишечные бактерии могут влиять на уровни нейромедиаторов».
Периферийный серотонин производится в желудочно-кишечном тракте энтерохромаффинными клетками, а также некоторыми типами иммунных клеток и нейронов. Сяо и её коллеги сначала постарались определить, влияют ли кишечные микроорганизмы на выработку серотонина в кишечнике, и если да, то в каком именно типе клеток. Учёные начали с измерения уровней периферийного серотонина у мышей с нормальным составом кишечных бактерий, а также у стерильных мышей, лишённых этих микроскопических резидентов.
Как оказалось, энтерохромаффинные клетки стерильных мышей производят примерно на 60% меньше серотонина, чем клетки их сородичей с обычным составом кишечных бактерий. Когда стерильным мышам вселили нормальные микробные колонии, уровень серотонина у них достиг нормы (то есть дефицит серотонина может быть обратимым).
«Энтерохромаффинные клетки являются богатым источником серотонина в кишечнике, – рассказывает Джессика Яно (Jessica Yano), соавтор исследования. – То, что мы увидели в ходе данного эксперимента, показывает: их способность производить серотонин или, по крайней мере, большая часть этой способности напрямую зависит от состава микробного сообщества кишечника».
Предыдущие исследования в этой области показали, что некоторые бактерии и вовсе могут производить «гормон счастья» сами по себе. Тем не менее данная научная работа предполагает, что большая часть серотонина в организме зависит от конкретных бактерий.
Подробности работы были опубликованы в журнале Сell
Кто в кишечнике производит нейромедиатор?
- Маргарита Паймакова, «Вести» по материалам Caltech: Microbes Help Produce Serotonin in Gut
- Хотя серотонин и известен как нейромедиатор мозга, по оценкам, около 90% от его общего количества в организме производится в желудочно-кишечном тракте.
- Изменения уровней этого так называемого периферийного серотонина связаны с различными заболеваниями, в том числе с синдромом раздражённого кишечника, сердечно-сосудистыми заболеваниями и остеопорозом.
- Новое исследование специалистов из Калифорнийского технологического института показало, что некоторые бактерии кишечника имеют большое значение для производства периферического серотонина.
«Всё больше и больше исследований показывают, что мыши и другие модельные организмы демонстрируют изменения в поведении в ответ на изменения в микробном составе их кишечников, – рассказывает Элейн Сяо (Elaine Hsiao), профессор биологии и биоинженерии и ведущий автор исследования. – Мы заинтересованы проследить взаимосвязь микробов и нервной системы. Для начала мы изучили, как кишечные бактерии могут влиять на уровни нейромедиаторов».
Периферийный серотонин производится в желудочно-кишечном тракте энтерохромаффинными клетками, а также некоторыми типами иммунных клеток и нейронов.
Сяо и её коллеги сначала постарались определить, влияют ли кишечные микроорганизмы на выработку серотонина в кишечнике, и если да, то в каком именно типе клеток.
Учёные начали с измерения уровней периферийного серотонина у мышей с нормальным составом кишечных бактерий, а также у стерильных мышей, лишённых этих микроскопических резидентов.
Как оказалось, энтерохромаффинные клетки стерильных мышей производят примерно на 60% меньше серотонина, чем клетки их сородичей с обычным составом кишечных бактерий. Когда стерильным мышам вселили нормальные микробные колонии, уровень серотонина у них достиг нормы (то есть дефицит серотонина может быть обратимым).
«Энтерохромаффинные клетки являются богатым источником серотонина в кишечнике, – рассказывает Джессика Яно (Jessica Yano), соавтор исследования. – То, что мы увидели в ходе данного эксперимента, показывает: их способность производить серотонин или, по крайней мере, большая часть этой способности напрямую зависит от состава микробного сообщества кишечника».
В дальнейшем исследователи решили выяснить, какие конкретные виды бактерий (или же всё разнообразие микробиома кишечника) взаимодействует с энтерохромаффинными клетками при производстве серотонина.
После тестирования различных видов и групп известных кишечных бактерий Яно и Сяо заметили, что за выработку серотонина у стерильных мышей отвечает одна группа из примерно 20 видов спорообразующих бактерий.
Мыши, которым вводилась эта группа микроорганизмов, также продемонстрировали изменения в активности тромбоцитов, которые, как известно, используют серотонин для свёртывания.
Также исследователям удалось выявить даже ряд конкретных молекул-метаболитов, регулирующих количество спорообразующих бактерий и повышающих уровни серотонина в культуре эмбриональных клеток.
Предыдущие исследования в этой области показали, что некоторые бактерии и вовсе могут производить «гормон счастья» сами по себе. Тем не менее данная научная работа предполагает, что большая часть серотонина в организме зависит от конкретных бактерий.
Несмотря на то, что серотонин важен для многих аспектов жизни человека, Сяо предупреждает: необходимо выполнить массу дополнительных исследований прежде, чем результаты данной работы могут быть применены при лечении людей.
«Мы определили группу бактерий, ответственную за увеличение уровней серотонина, однако есть вероятность, что она ответственна и за различные другие эффекты – это нам ещё предстоит выяснить, – рассказывает исследовательница. – Кроме того, существуют ситуации, при которых избыток периферического серотонина может принести вред организму».
Подробности работы были опубликованы в журнале Cell (Yano et al., Indigenous Bacteria from the Gut Microbiota Regulate Host Serotonin Biosynthesis).
Портал «Вечная молодость» http://vechnayamolodost.ru16.04.2015
Полезные бактерии в организме человека
Полезные бактерии в организме человека
Совокупность бактерий, населяющих человеческий организм, имеет общее название – микробиота. В нормальной, здоровой микрофлоре человека насчитывается несколько миллионов бактерий. Каждая из них играет важную роль для нормального функционирования человеческого тела.
При отсутствии какого-либо вида полезных бактерий человек начинает заболевать, нарушается работа ЖКТ, дыхательных путей. Полезные бактерии для человека концентрируются на коже, в кишечнике, на слизистых оболочках тела.
Количество микроорганизмов регулируется с помощью иммунной системы.
В норме, тело человека содержит как полезную, так и патогенную микрофлору. Полезных бактерий намного больше. Они составляют 99% от общего числа микроорганизмов. При таком положении соблюдается необходимый баланс. Среди разных видов бактерий, обитающих на теле человека можно выделить:
бифидобактерии; лактобактерии; энтерококки; кишечная палочка.
Бифидобактерии
Этот вид микроорганизмов самый распространённый, участвует в процессе выработки молочной кислоты и ацетата. Он создаёт кислую среду, этим самым нейтрализует большинство болезнетворных микробов. Патогенная флора перестаёт развиваться и вызывать процессы гниения и брожения.
Бифидобактерии играют важную роль в жизни ребёнка, так как именно они отвечают за наличие аллергической реакции на какие-либо пищевые продукты. Кроме того они оказывают антиоксидантное действие, предотвращают развитие опухолей.
Синтез витамина С не обходится без участия бифидобактерий. К тому же, есть информация, что бифидобактерии помогают усваиваться витаминам D и B, которые необходимы человеку для нормальной жизнедеятельности.
При наличии дефицита бифидобактерий даже приём синтетических витаминов этой группы не принесёт никакого результата.
Лактобактерии
Эта группа микроорганизмов также важна для здоровья человека. Благодаря их взаимодействию с другими обитателями кишечника блокируется рост и развитие патогенных микроорганизмов, подавляются возбудители кишечных инфекций. Лактобактерии участвуют в образовании молочной кислоты, лизоцина, бактериоцинов.
Это отличная помощь иммунной системе. Если в кишечнике есть дефицит этих бактерий, то очень быстро развивается дисбактериоз. Лактобактерии заселяют не только кишечник, но и слизистые. Так эти микроорганизмы важны для женского здоровья.
Они поддерживают кислотность среды влагалища, не допускают развития бактериального вагиноза.
Кишечная палочка
Не все виды кишечной палочки являются болезнетворными. Большинство из них наоборот выполняют защитную функцию. Полезность рода кишечная палочка состоит в синтезе коцилина, который активно противостоит основной массе патогенной микрофлоры.
Данные бактерии полезны для синтеза разных групп витаминов, фолиевой и никотиновой кислоты. Нельзя недооценивать их роль для здоровья.
Например, фолиевая кислота необходима для производства красных кровяных телец и поддержания нормального уровня гемоглобина.
Энтерококки
Этот вид микроорганизмов заселяет кишечник человека сразу после рождения. Они помогают усваиваться сахарозе.
Обитая в основном в тонком кишечнике, они, как и другие полезные не патогенные бактерии обеспечивают защиту от чрезмерного размножения вредоносных элементов. В то же время, энтерококки относятся к условно безопасным бактериям.
Если они начинают превышать допустимые нормы, развиваются разные бактериальные заболевания. Список болезней очень большой. Начиная от кишечных инфекций, заканчивая менингитом.
Положительное влияние бактерий на организм
Полезные свойства не патогенных бактерий очень многообразно. До тех пор пока существует баланс между обитателями кишечника и слизистых, организм человека нормально функционирует. Большинство бактерий участвует в процессах синтеза и расщепления витаминов.
Без их присутствия витамины группы В не усваиваются кишечником, что приводит к нарушениям со стороны нервной системы, заболеваниям кожи, понижению гемоглобина. Основная масса не переваренных компонентов пищи, достигших толстого кишечника, расщепляется именно благодаря бактериям.
Кроме того, микроорганизмами обеспечивается постоянство водно-солевого обмена. Более половины всей микрофлоры участвует в регуляции всасывания жирных кислот, гормонов. Микрофлора кишечника формирует местный иммунитет. Именно здесь происходит уничтожение основной массы патогенных организмов, блокируется вредоносный микроб.
Соответственно, люди не ощущают вздутия и метеоризма. Увеличение лимфоцитов провоцирует активные фагоциты для борьбы с врагом, стимулируют продуцирование иммуноглобулина А.
Полезные не патогенные микроорганизмы положительно влияют на стенки тонкого и толстого кишечника. Они поддерживают там постоянный уровень кислотности, стимулируют лимфоидный аппарат, эпителий становится устойчивым к разным канцерогенам. Перистальтика кишечника также во многом зависит от того, какие бывают микроорганизмы в нём.
Подавление процессов гниения и брожения – одна из основных задач бифидобактерий. Многие микроорганизмы долгие годы развиваются в симбиозе с болезнетворными бактериями, тем самым, контролируя их. Биохимические реакции, которые постоянно происходят с бактериями, выделяют много тепловой энергии, поддерживая общий тепловой баланс организма. Питаются микроорганизмы не переваренными остатками.
Дисбактериоз
Дисбактериоз – это изменение количественного и качественного состава бактерий в организме человека. При этом полезные организмы погибают, а вредоносные активно размножаются. Дисбактериоз затрагивает не только кишечник, но и слизистые (может быть дисбактериоз ротовой полости, влагалища). В анализах будут превалировать названия: стрептококк, стафилококк, микрококк.
В нормальном состоянии полезные бактерии регулируют развитие патогенной микрофлоры. Кожные покровы, органы дыхания обычно находятся под надёжной защитой. Когда нарушается баланс, человек ощущает следующие симптомы: метеоризм кишечника, вздутие, боли в животе, расстройство. Позже может начаться снижение веса, анемия, авитаминоз.
Со стороны половой системы наблюдаются обильные выделения, часто сопровождающиеся неприятным запахом. На коже появляются раздражения, шероховатости, трещинки. Дисбактериоз — побочное действие после приёма антибиотиков. При обнаружении подобных симптомов нужно обязательно обратиться к врачу, который назначит комплекс мероприятий по восстановлению нормальной микрофлоры.
Часто для этого требуется приём пробиотиков.
Поделиться в соц. сети