ПостНаука
Невролог Марина Нодель о синдроме паркинсонизма, дефиците дофамина и разработке методов нейропротекции
Болезнь Паркинсона – хроническое прогрессирующее нейродегенеративное заболевание головного мозга. Описания проявлений болезни были обнаружены еще в трудах древнеиндийских врачей – Аюрведе.
Но первооткрывателем заболевания признан английский врач Джеймс Паркинсон, выпустивший в 1817 году труд «Эссе о дрожательном параличе», где описал несколько случаев и отметил ряд характерных симптомов болезни.
Более полное описание клинической картины заболевания сделал в 1860-е годы французский невролог Жан Мартен Шарко, он и предложил назвать заболевание в честь Джеймса Паркинсона.
Симптомы болезни Паркинсона
Синдром паркинсонизма является ключевым в клинической картине заболевания. Он проявляется замедлением темпа и снижением амплитуды движений (брадикинезией) в сочетании с повышением тонуса мышц и/или дрожанием (тремором) рук, ног, подбородка. Ключевым нарушением является именно брадикинезия, а тремор в четверти случаев болезни вовсе отсутствует.
Брадикинезия может проявляться снижением громкости голоса и нарушением артикуляции, обеднением мимики, уменьшением размера букв при письме, ограничением выполнения мелких движений пальцами рук, паркинсонической походкой (снижением высоты и длины шага), замедлением и затруднением вставания со стула, поворотов в постели.
Брадикинезия, изменения мышечного тонуса и позы нередко проявляются болями или неприятными ощущениями в руке (плечевом суставе), спине. С синдромом паркинсонизма на поздних стадиях болезни сочетается неустойчивость с возможными падениями, нарушениями начала ходьбы, эпизодами непроизвольных остановок («застываний») при ходьбе.
Выделяют форму, где преобладает тремор (преимущественно дрожательную форму), акинетико-ригидную (без тремора) и смешанную.
Замечено, что акинетико-ригидная форма зачастую протекает более тяжело – с относительно быстрым нарастанием нарушений ходьбы, неустойчивости, расстройств в интеллектуальной сфере.
Болезнь Паркинсона отличается значительной вариабельностью течения заболевания с разной степенью выраженности двигательных и недвигательных проявлений.
Причины болезни Паркинсона
Однозначного ответа на вопрос о первопричине возникновения болезни Паркинсона пока нет. Исследователи продолжают изучать причины преждевременного старения и гибели нервных клеток.
Полагают, что развитие болезни вызвано взаимодействием наследственной предрасположенности, внешних нейротоксических факторов и процессов старения.
Некоторые наследуемые гены усиливают уязвимость нервных клеток к воздействию повреждающих факторов внешней среды.
К внешним вредным факторам относят соли некоторых металлов, органические растворители, пестициды и гербициды. Список веществ, потенциально опасных для нервных клеток, продолжает расширяться.
В результате этого взаимодействия запускается каскад невропатологических реакций.
Так формируется распространенный нейродегенеративный процесс, поражающий по мере прогрессирования заболевания различные отделы головного мозга и периферической вегетативной нервной системы.
Тельца Леви
Важная веха в изучении болезни Паркинсона связана с открытием морфологического субстрата болезни.
В 1919 году советский невропатолог Константин Третьяков связал развитие симптомов паркинсонизма с утратой особых клеток мозга – пигментных нейронов черной субстанции ствола, а также с отложением в этих клетках патологических включений.
Нейрональные включения Третьяков предложил называть тельцами Леви в честь немецкого морфолога Фридриха Леви, который ранее описал схожие изменения при паркинсонизме в других отделах ствола мозга. Это открытие является основополагающим в понимании патологических изменений, лежащих в основе двигательных симптомов заболевания.
Дефицит дофамина
Возникновение двигательных проявлений болезни Паркинсона связано с преждевременной гибелью нервных клеток мозга, вырабатывающих дофамин. В 1958 году шведский фармаколог Арвид Карлссон, проводя опыты на животных, доказал значимую роль дофамина в головном мозге.
Спустя полвека он получил за это открытие Нобелевскую премию. Значительное снижение содержания дофамина в срединных структурах головного мозга (базальных ганглиях) у пациентов, умерших от болезни Паркинсона, было показано в 1961 году австрийским ученым Олегом Горникевичем.
Дофамин – это нейрохимическое вещество, необходимое для передачи нервных импульсов в клетках мозга, обеспечивающих способность к движению. Нехватка дофамина, в свою очередь, является основной причиной двигательных нарушений у пациентов.
Однако дефицит выработки дофамина проявляется не только нарушениями в двигательной сфере. Дофамин участвует в регуляции эмоций, мотивационных компонентов поведения, познавательных процессов.
Поэтому для болезни Паркинсона весьма характерны расстройства эмоциональной, интеллектуальной сферы, поведения.
Морфология при болезни Паркинсона
В последние десятилетия представления о морфологии при болезни Паркинсона были значительно расширены, получены свидетельства распространенности патологического процесса при этом заболевании.
Помимо дефицита дофамина, доказано «страдание» и других нейрохимических систем мозга.
Так, с дегенерацией ядер ствола мозга, вырабатывающих иные нейромедиаторы (серотонин, норадреналиин, ацетилхолин), связано развитие депрессии, тревоги, апатии, расстройств ночного сна и повышенной дневной сонливости, нарушение интеллектуальных функций.
Эти симптомы в разных сочетаниях на разных стадиях заболевания встречаются у 30–80 % больных и могут опережать двигательные классические симптомы болезни на 5–10 лет, формируя так называемую додвигательную стадию заболевания. Болезнь Паркинсона может начаться с недофаминергических структур мозга.
Методы диагностики
Диагноз «болезнь Паркинсона» устанавливается на основе анализа истории болезни – анамнеза и данных клинического осмотра.
Нейровизуализация головного мозга (магнитно-резонансная томография) используется для исключения других заболеваний (опухоли мозга, гидроцефалии, дисциркуляторной энцефалопатии) и назначается главным образом при обнаружении атипичных, нехарактерных для болезни Паркинсона анамнестических данных или клинических симптомов.
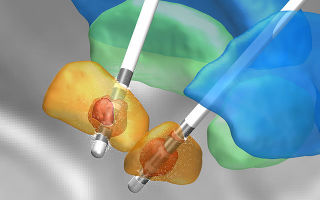
Современные методы нейровизуализации (однофотонная эмиссионная компьютерная томография, позитронно-эмиссионная томография) с введением различных радиофармпрепаратов позволяют оценить функциональное состояние окончаний нейронов, вырабатывающих дофамин в мозге, по степени поглощения радиоактивных аналогов дофамина. Эти методы применяются главным образом в научных исследованиях, могут использоваться в диагностически сложных случаях. Но дороговизна современных методов нейровизуализации не позволяет широко применять их в клинической практике.
Для подтверждения диагноза «болезнь Паркинсона», особенно при начальных проявлениях, может быть проведено ультразвуковое исследование – транскраниальная сонография.
При этом маркером болезни Паркинсона является повышение интенсивности сигнала (гиперэхогенности) от черной субстанции (чувствительность и специфичность метода составляет 90 %).
В отличие от функциональных методов нейровизуализации, транскраниальная сонография отличается безопасностью и простотой: не вводятся внутривенно радиофармпрепараты. Она доступна с экономической точки зрения.
Терапия болезни Паркинсона
Основной подход к терапии болезни Паркинсона – симптоматический, то есть воздействие на симптомы болезни с целью уменьшения степени их тяжести. Новая эра в лечении пациентов с болезнью Паркинсона началась в 1960-х годах, когда начали применять леводопу – это метаболический предшественник дофамина.
Препараты, содержащие леводопу, до сих пор являются наиболее эффективными средствами для лечения болезни Паркинсона. Применяются и другие средства, функционально замещающие недостаток дофамина: агонисты дофаминовых рецепторов, амантадины, препараты, уменьшающие разрушение (катаболизм) дофамина и леводопы.
Лечебная программа каждого пациента разрабатывается индивидуально с учетом степени функциональной дезадаптации, возраста, выраженности отдельных симптомов болезни, наличия побочных эффектов терапии и сопутствующих заболеваний.
Задачей терапии является максимальное восстановление повседневной активности при использовании минимально возможных доз безопасных для пациента препаратов.
В случае недвигательных проявлений болезни – депрессии, нарушений сна – требуется оценка характера и тяжести симптомов и соответствующая им терапия.
Хирургическое лечение (электрическая стимуляция глубинных структур мозга, вовлеченных в заболевание) применяется на развернутых стадиях болезни в тех случаях, когда возможности лекарственной терапии ограничены в результате прогрессирования болезни или нежелательных явлений терапии. Операции позволяют уменьшить проявления болезни и снизить дозы лекарственной терапии. Большое значение придается двигательной активности. Доказано, что регулярная дозированная физическая нагрузка способствует более благоприятному течению заболевания.
Современные исследования паркинсонизма
Современные исследования болезни Паркинсона охватывают самые разные аспекты. Одно из активно разрабатываемых направлений изучения болезни Паркинсона – уточнение молекулярных механизмов патогенеза заболевания, выделение биохимических, клинических маркеров ранних этапов развития заболевания.
Понимание данных аспектов перспективно в отношении разработки и внедрения эффективных методов нейропротекции – подходов, направленных на замедление нейродегенерации. Изучаются генетические, морфофункциональные, клинические факторы, позволяющие прогнозировать особенности течения заболевания.
Уточняются этиологические особенности патофизиологии недвигательных расстройств заболевания, степень их влияния на качество жизни пациентов, подходы к их профилактике и лечению.
Для симптоматической терапии разрабатываются более совершенные лекарственные формы, обеспечивающие длительную, физиологическую активацию дофаминергических рецепторов базальных ганглиев.
Предпосылками для этой задачи являются особенности фармакокинетики леводопы с непродолжительным периодом полувыведения препарата из плазмы крови, замедление моторики желудочно-кишечного тракта у пациентов с болезнью Паркинсона с нарушением всасывания препарата на поздних стадиях болезни.
Об авторе: Марина Нодель – доктор медицинских наук, доцент кафедры нервных болезней лечебного факультета, ведущий научный сотрудник НИО Неврологии Первого МГМУ им. Сеченова, руководитель Центра болезни Паркинсона и двигательных расстройств Российского Научно-клинического Геронтологического Центра.
Портал «Вечная молодость» http://vechnayamolodost.ru 01.03.2017
Профилактика болезней Альцгеймера и Паркинсона
25 июня 2019.
Рост продолжительности жизни и новые привычки дали человечеству возможность познакомиться с болезнью Альцгеймера, которая похищает воспоминания, обыденные навыки и личность.Она возникает из-за аномального накопления определенных белков в клетках мозга и межклеточном пространстве.
Бляшки с фрагментами бета-амилоида оседают в промежутках между нервными клетками, блокируя связь между ними. Другой, под названием тау-белок, в мозге здорового человека стабилизирует компоненты каркаса, что поддерживает клетки целыми.
Во время молекулярных изменений он становится токсичным, начинает слипаться между собой, образуя разрушительные для нейронов нейрофибрилярные клубки. Эти изменения начинаются за много лет до появления первых симптомов.
Триггерами заболевания являются один или совокупность факторов. Прежде всего – возраст: после 65 лет риск удваивается каждые пять лет, после 80 лет болезнь встречается у каждого шестого, после 85-ти – каждого третьего, у каждого второго после 90 лет. Существуют и половые различия – женщины чаще болеют болезнью Альцгеймера, особенно после 85 лет.
Заболевание отбирает у человека восемь жизненно необходимых навыков: память, речь, ориентировку в пространстве, времени и собственной личности, способность адекватно воспринимать окружающее, конструктивные способности, умение решать обыденные проблемы, функционирование, способность самообслуживания.
Можно ли предотвратить Альцгеймер? Эксперты соглашаются, что в подавляющем большинстве случаев эта болезнь, как и другие хронические заболевания, вероятно, развивается в результате сложных взаимодействий между различными факторами, включая возраст, генетику, окружающую среду, образ жизни и сопутствующие заболевания.
Такие факторы, как возраст или гены не могут быть изменены, однако, все остальные можно минимизировать, чтобы уменьшить риск появления Альцгеймера. Основная задача превентивных шагов – улучшить когнитивные процессы, способствовать построению новых нейронных связей в мозгу.
Болезнь Альцгеймера – это заболевание, при котором мозг утрачивает свои функции вследствие гибели клеток и нарушения нейронных связей. Однако доказан факт, что мозг человека достаточно пластичен, клетки и отделы мозга могут частично заменять пораженные области, выполняя дополнительные функции.
Для того, чтобы предоставить мозгу возможность к подобной самокомпенсации, количество нейронных связей должно быть достаточно высоким, что происходит у людей с умственным видом деятельности, интеллектуальными хобби, разнообразием интересов.
Исследования доказывают, что болезнь Альцгеймера напрямую коррелирует с уровнем IQ: чем выше интеллект, а значит, количество устойчивых нейронных связей в мозге, тем реже проявляется заболевание.
Известно также о зависимости между изучением иностранных языков и развитием старческой деменции: чем больше знаний, тем ниже риски заболеть. Даже при начальной стадии заболевания можно замедлить развитие симптомов, если активно начать тренировать память, читать и пересказывать информацию, решать кроссворды.
- Тренировка мозга: изучение новой информации (слов, стихов), интеллектуальные игры, игра на музыкальных инструментах и даже выполнение привычных ритуалов левой рукой или изменение маршрута на работу, позволяют укрепить нейронные сети мозга и замедляют их ослабление в процессе старения. Эти шаги снижают риск заболевания в 2,4 раза.
- Специальное питание: сбалансированный рацион с низким гликемическим индексом предотвращает не лишь сердечно-сосудистым болезням и появление диабета, но и деменции. Для здоровья мозга и всего организма в ежедневном рационе должны быть нежирные виды мяса, морская рыба, продукты из цельного зерна, яйца, фрукты и овощи, особенно зелень, орехи, бобовые, кисломолочные продукты, качественные жиры. Стоит избегать избытка углеводов, жареной пищи, трансжиров и сладостей, ведь потребление 30 граммов сахара в день повышает риск заболевания на 33%.
- Спорт и физическая активность: для профилактики Альцгеймера не нужно часами пропадать в тренировочном зале, гораздо важнее регулярно и умеренно нагружать тело различными видами активностей. Это могут быть пешие прогулки, бег, занятия спортом несколько раз в неделю, танцы. Ученые утверждают, что таким образом не только повышается тонус мышц, кровоснабжение всего тела, но и улучшаются когнитивные функции.
- Социализация и ощущение счастья: одиночество, хронический стресс и депрессия повышают вероятность развития Альцгеймера, поскольку из-за высокого уровеня кортизола (гормона стресса) уменьшаются области мозга, отвечающие за память. Поэтому общение, дружба и самореализация для пожилых людей не менее важны, чем в младшем возрасте.
Болезнь Паркинсона
Речь идет о заболевании нервной системы, при котором постепенно разрушаются нейроны, вырабатывающие один из важнейших нейромедиаторов — дофамин. Чаще всего болезнь Паркинсона поражает людей в возрасте — в 55–65 лет. Однако известны случаи, когда болезнь диагностировалась у молодых людей в возрасте 30–40 лет. Существует и так называемая ювенильная форма, при которой заболевание поражает подростков в возрасте до 20 лет. Стоит сказать, что мужчины страдают от болезни Паркинсона чаще, чем женщины, хотя объективных причин этого факта наука еще не выявила.Прижизненная диагностика с целью определения количества нежизнеспособных дофаминергических нейронов также практически невозможна. Классическому течению болезни как основному источнику постановки корректного диагноза на болезнь Паркинсона свойственны четыре группы специфических клинических признаков:
- тремор скелетных мышц конечностей и туловища (неконтролируемые однотипные движения с частотой колебания 4-6 Гц). Благодаря специфическому дрожанию, болезнь Паркинсона получила второе название – дрожательный паралич,
- постуральная неустойчивость (нарушение координации движения во время стоячей позы или при движении),
- ригидность скелетной мускулатуры (повышенный их тонус, напряжение),
- брадикинезия (замедленность физической реакции на окружающую действительность, заторможенность).
На сегодняшний день не существует клинических и лабораторных методов выявления болезни Паркинсона на ранних стадиях, поэтому лечение в латентном периоде заболевания не представляется возможным.
К моменту проявления первых клинических признаков, поражено уже более половины нервных клеток-продуцентов дофамина, восстановление которых невозможно.
К возможным причина развития болезни Паркинсона относят — наследственный фактор, черепно-мозговые травмы, разного рода интоксикации, отравления химическими веществами, ожирение, хронические мигрени, острые отравления тяжелыми металлами.
В силу развития и протекания, не существует специфических мер профилактики данного заболевания. Феномен паркинсонизма заключается в том, что болезнь может возникнуть спонтанно, без видимых определенных причин, причем на момент установки диагноза, происходят весьма значительные и, самое главное, необратимые изменения в головном мозге, что и делает болезнь неизлечимой.
Исходя из данных особенностей болезни, условно существуют мероприятия, упреждающие дальнейшее активное развитие болезни либо предупреждающие о ее вероятном появлении:
- Классическая форма болезни Паркинсона заключена в ее наследственности. Поэтому при наличии утвержденных диагнозов в семейном древе, существует вероятность рецидива у потомков.
- Долгий прием (более одного месяца) нейролептических препаратов способствует развитию лекарственной формы паркинсонизма.
- Сосудистые патологии в головном мозге нативной этиологии или вследствие посттравматических либо постинфекционных явлений, могут провоцировать дисфункцию выработки дофамина нейронами головного мозга.
- Появление клинических признаков, свойственных паркинсонизму, даже в единственном количестве, служит серьезным поводом для обращения к врачу с целью дифференциации болезни Паркинсона от заболеваний, сходных по клинике.
- В молодом и среднем возрасте существуют некоторые признаки, отличающиеся от классических и сигнализирующих о возможном начале болезни Паркинсона: неусидчивость при выполнении работы, повышенная реакция на раздражители, неадекватные угловатые движения, неспособность выполнить какие-то более сложные физические действия, нелогичность мимической реакции на происходящее. У детей частым клиническим признаком является своеобразное выгнутое положение тела при походке с характерным прижатием рук к поясу или бедрам, в отличие от здоровых людей, когда руки раскачиваются в такт ходьбе.
- Научно, практически, доказанный факт – болезнь Паркинсона практически не встречается у курильщиков и любителей кофе. Однако, непосредственно на стадиях болезни курение и прием кофе не оказывает никакого терапевтического эффекта.
- флавоноиды и антоцианы – вещества, обладающие выраженным нейрозащитным эффектом. Больше всего этих веществ содержится в яблоках и цитрусовых,
- здоровый, физически и умственно полноценный образ жизни человека, избегание стрессов – значимые факторы, предупреждающие патологии нервной системы, повышающие планку ее защитного барьера,
- при отсутствии отдельный противопоказаний, регулярный прием натурального кофе, бережное отношение к своему здоровью в плане физических повреждений головы, ограничение контактов с вредными веществами, диета, богатая витаминами группы В и постоянное занятие физкультурой значительно снижает риск болезни Паркинсона при условии отсутствия генетической расположенности.
Отделение функциональной диагностики
врач Бяко И.В.
Два компонента кофе защитили нейроны при болезни Паркинсона
Тельце Леви, состоящее из альфа-синуклеина
Wikimedia Commons
Исследователи частично объяснили защитный эффект кофе,
который проявляется в снижении риска развития нейродегенеративных заболеваний, совместным
действием двух его компонентов.
Как показали авторы статьи в PNAS, продолжительное потребление модельными мышами с
болезнью Паркинсона низких доз кофеина и эйкозанил-5-гидрокситриптамида
облегчило у животных поведенческие симптомы и снизило количество
фосфорилированного α-синуклеина в нейронах.
По-видимому, оба эти компонента
кофе действуют через разные механизмы на одну и ту же мишень — фермент, который
препятствует накоплению синуклеина.
Болезнь Паркинсона — тяжелое нейродегенеративное заболевание,
обусловленное гибелью дофаминэргических нейронов в результате образования в них
скоплений белка α-синуклеина (эти скопления еще называются тельцами Леви).
В
норме растворимый белок, α-синуклеин начинает «склеиваться» и образовывать
опасные агрегаты при навешивании на него остатка фосфорной кислоты
(модификация, называемая фосфорилированием).
Удалением фосфатов как с
синуклеина, так и с других белков, ассоциированных с нейродегенеративными заболеваниями,
занимается фермент фосфатаза PP2A. Показано, что при болезни
Паркинсона ее активность в нейронах снижена.
Эпидемиологические исследования на людях неоднократно
связывали снижение риска развития нейродегенеративных заболеваний, в том числе
болезни Паркинсона, с регулярным потреблением кофе. Исследовательская группа из
Медицинской
школыимени
Роберта
Вуда Джонсона (Нью-Джерси,
США) под руководством Марала Мурадяна (M.
Maral Mouradian) занимается изучением
связи кофе и нейродегенерации на молекулярном уровне. Ранее ученые уже показали,
что один из компонентов кофе, эйкозанил-5-гидрокситриптамид, ингибирует
фермент, подавляющий активность фосфатазы PP2A.
У модельных
мышей, которым в пищу в больших дозах добавляли это вещество в течение девяти
месяцев, симптомы заболевания были выражены значительно слабее, за счет повышения
активности PP2A и снижения накопления
синуклеина.
Эйкозанил-5-гидрокситриптамид — производная серотонина, где к аминогруппе присоединен остаток эйкозановой (арахиновой) жирной кислоты. Компонент липидной фракции кофе и кофе-масла
Wikimedia Commons
Основной действующий компонент кофе — кофеин, также был
замечен в предотвращении агрегации α-синуклеина. В новой работе американские
исследователи показали, что кофеин и эйкозанил-5-гидрокситриптамид в паре даже
в низких дозах проявляют защитный эффект по тому же самому механизму.
Эксперимент проводили на генно-модифицированных мышах с
болезнью Паркинсона (у них в нейронах экспрессировался человеческий α-синуклеин).
В норме через несколько месяцев после рождения у них уже проявляются
поведенческие симптомы заболевания (изменение походки, когнитивные нарушения и
так далее).
Мыши, которым с рождения в пищу добавляли низкие субтерапевтические
дозы обоих веществ, через шесть месяцев проходили поведенческие тесты
значительно лучше, чем контрольные мыши. Активность фермента у них в мозге была
повышена, а агрегации α-синуклеина почти не наблюдалось.
При этом по
отдельности оба компонента в такой концентрации защитного эффекта не проявляли.
Накопление фосфорилированного альфа-синуклеина в коре (А) и гиппокампе (B) обычных мышей (WT) и мышей с болезнью Паркинсона (SynTg). CAF — кофеин, EHT — эйкозанил-5-гидрокситриптамид
Run Yan et al / PNAS 2018
Обсуждая механизм наблюдаемого эффекта, авторы предположили,
что компоненты через разные пути действуют на одну и ту же мишень — PP2A. Если эйкозанил-5-гидрокситриптамид
ингибирует снижение ее активности путем метилирования, кофеин, вероятно,
проявляет действие через подавление аденозиновых рецепторов, так как в одном из
предшествующих экспериментов полное удаление этих рецепторов тоже защитило
мышей от нейродегенерации.
В завершение авторы подчеркивают, что кофе содержит около
тысячи активных компонентов, которые могут проявлять взаимодополняющий эффект.
Приведенная пара веществ, вероятно, вносит вклад в суммарное влияние кофе на
потребителя, но вряд ли дело ограничивается только ей.
О том, как кофе влияет на разных людей в зависимости от
генотипа и привычек, можно прочитать в нашем блоге «Проклятье четырех чашек».
Дарья Спасская
Можно ли предотвратить болезнь Паркинсона?
11 апреля отмечается Всемирный день борьбы с болезнью Паркинсона – медленно прогрессирующим хроническим заболеванием, связанным с гибелью нейронов — нервных клеток в головном мозге.
В основном заболеванию подвержены пожилые люди старше 60 лет. По статистике примерно у одного человека из ста обнаруживается данное заболевание. Из-за повреждения клеток начинаются проблемы с регуляцией движения и тонусом мышц.
На ранних сроках болезнь Паркинсона тяжело обнаружить, так как заметные клинические симптомы проявляются лишь на поздних стадиях заболевания. Начальный период болезни может длиться не одно десятилетие.
Нейроны умирают неравномерно, и мозг не сигнализирует о проблеме. Людям, чьи родственники имеют данное заболевание важно внимательно следить за здоровьем, так как болезнь может передаваться по наследству.
Специалисты отмечают несколько признаков, которые могут указывать на заболевание.
Возможные признаки болезни Паркинсона
Данные симптомы не означают обязательное наличие заболевания, но если вы или ваши близкие имеете предрасположенность к болезни, обязательно проконсультируйтесь с врачом при обнаружении совокупности подобных признаков.
Ухудшение обоняния
На ранней стадии заболевания можно заметить проблемы распознавания запахов. Это связано с нарушением стабильной работы определенной доли мозга, которая влияет на возможность ощущать запахи. Этот симптом является самым ранним и прослеживается ещё за пару лет до появления других нарушений.
Депрессия, меланхолия и апатия
Подавленное психическое состояние является достаточно распространенным симптомом болезни. Депрессия встречается у пациентов с болезнью Паркинсона чаще, чем у пациентов такого же возраста и пола с другими заболеваниями, кроме того риск развития болезни у человека с имеющимся расстройством психики выше более чем в три раза.
Нарушение речи или памяти
Нарушение памяти является нередким случаем среди людей преклонного возраста, поэтому на этот признак редко обращают внимание. Более заметным является нарушение речи. Человек утрачивает способность проявлять какие-либо эмоции голосом: он не может разговаривать на разных тонах, голос становится более тихим, а при повторении фраз человек начинает нервничать, запинаться.
Проблемы со сном
К симптомам может относиться фрагментация сна и раннее пробуждение по утрам. Также отмечаются крупноамплитудные движения руками и ногами во время фазы «быстрого сна».
Тремор конечностей
Дрожание рук или других конечностей является характерным признаком болезни Паркинсона, но уже на более поздних стадиях. Его проявление становится наиболее заметным в стрессовых ситуациях. Сам человек может не ощущать этого непроизвольного движения.
Берегите свое здоровье!
К сожалению, болезнь Паркинсона практически не поддается лечению, но при правильно поставленном диагнозе и верной терапии, выполнении физиотерапевтических процедур и здоровом образе жизни развитие болезни можно замедлить. В случае если вы имеете предрасположенность к болезни, специалисты рекомендуют избегать ряда факторов:
- Остерегайтесь экстремальных видов спорта и других активностей, при которых возможен риск получения травмы головы;
- Избегайте контакта с вредными химическими веществами (работа на производстве, использование удобрений, концентрированной бытовой химии и т.д.);
- Избегайте стрессовых ситуаций и старайтесь получать больше положительных эмоций;
- Контролируйте уровень половых гормонов и повышение в крови гомоцистеина – аминокислоты, способствующей развитию болезни.
Заботьтесь о себе и своих близких!
Паркинсонизм
У паркинсонизма есть ряд характерных симптомов, которые позволяют четко дифференцировать это заболевание:
- Дрожание конечностей и головы. Особенность в том, что тремор возникает в состоянии покоя и затихает при попытках движения.
- Мышечная скованность, напряжение, гипертонус. Усиливается при повторных однообразных движениях, пациенту сложно выполнять их длительное время.
- Характерная для паркинсонизма поза: спина сгорблена, конечности поджаты к туловищу, голова все время наклонена вперед.
- Нетвердая семенящая походка – пациент передвигается мелкими шажками, плохо отрывает стопу от пола.
- При паркинсонизме пациенты часто падают, теряют равновесие.
- Двигательная бедность – сложно начать движение, они замедленны.
- Снижается мимическая активность.
- Речь становится тихой, монотонной.
- У пациента заметно беднеет память, есть нарушения мышления.
- Психологические расстройства – сниженное настроение, склонность к критике.
- Кожа становится сальной.
- Повышается слюноотделение, у некоторых пациентов можно заметить выраженное слюнотечение.
- Есть еще одна характерная особенность – склонность к запорам, редкий стул, нарушение перистальтики.
Даже характерные симптомы не гарантируют достоверную диагностику. Поэтому необходимо пройти полноценное обследование.
В ЦЭЛТ вы можете получить консультацию специалиста-невролога.
- Первичная консультация — 3400
- Повторная консультация — 2100
Записаться на прием
Формы
Выделяют два основных типа паркинсонизма:
- Первичный. Это болезнь Паркинсона, самостоятельное заболевание. Может быть ассоциировано с другими болезнями, но не вызвано ими.
- Вторичный. Возникает на фоне травмы, отравления, другого заболевания. Является последствием, а не причиной. Соответственно, для лечения требуется иной подход.
Выделяют несколько форм вторичного заболевания, которые классифицируют исходя из предпосылок заболевания.
- Инфекционный паркинсонизм – развивается после перенесенной инфекции. Чаще всего в роли провоцирующих заболеваний выступают энцефалиты, грипп, сифилис.
- Сосудистый – развивается в постинсультный период. Может быть вызван хроническим нарушением мозгового кровообращения.
- Токсический – последствие приема или воздействия различных токсинов. Одна из форм – лекарственная – развивается на фоне приема фармацевтических препаратов.
- Травматический – последствия травмы головы. Может возникать при регулярных травмах головы, например, у спортсменов – борцов, боксеров.
- Опухолевый – вызван опухолями головного мозга.
- Идиопатический – так называют болезни, причину которых не удалось установить достоверно. Если есть полный симптомокомплекс синдрома Паркинсона, то ставят этот диагноз, несмотря на отсутствие явной причины.
Причины
Основная причина заболевания – это отмирание нейронов в области головного мозга, которая отвечает за координированное действие мышц и мышечный тонус.
Также неврологи отметили недостаток дофамина в этой области мозга, который вызывает такие симптомы, как тремор и мышечная скованность. А вот факторов риска или предпосылок довольно много.
Они не обязательно напрямую приводят к развитию заболевания, но значительно повышают его вероятность.
Выявить точную причину может только врач-невролог после полноценного обследования.
Диагностика
Сначала врач собирает анамнез. Пациенту задают такие вопросы:
- Как давно появились первые симптомы и как быстро они прогрессировали?
- Усиливается ли тремор в покое?
- Есть ли наследственные предпосылки к развитию заболевания?
- Работает ли пациент на производствах с повышенной токсической опасностью?
- Принимает ли пациент лекарственные препараты, повышающие риск развития паркинсонизма?
- Были ли в недавнем прошлом тяжелые эпизоды инфекционных заболеваний?
- Были ли травмы головы?
Затем врач проводит стандартный для подобных жалоб неврологический осмотр: оценивает походку, мышечный тонус, характер тремора и т.д.
Следующий этап – фармакологический тест. Он заключается в назначении пациенту препарата на основе дофамина или аналогичных веществ. Если есть паркинсонизм, то это способствует снижению симптоматики.
Нередко требуется консультация психолога для оценки когнитивной и эмоциональной сферы. Обычно для этого используют стандартные тесты и опросники.
Подтвердить диагноз можно на МРТ – обследование покажет патологические участки в области, отвечающей за мышечный тонус и координацию. Эти высветленные участки показывают отмершие нейроны. МРТ позволяет также подтвердить или исключить опухоль.
Диагностика заканчивается постановкой диагноза, в соответствии с которым назначают лечение.
Лечение паркинсонизма
Лечение сходно и для синдрома Паркинсона, и для болезни Паркинсона. Главное отличие заключается в том, что при синдроме требуется установить причину и начать лечение основного заболевания.
Рекомендуются следующие методы лечения:
- Назначаются препараты с содержанием дофамина или его предшественников.
- Препараты, которые тормозят разрушение дофамина.
- Нейропротекторы – защищают нейроны от гибели.
- Антидепрессанты – при серьезных нарушениях эмоциональной сферы.
- Лечебная физкультура – способна снизить симптоматику на ранних стадиях.
- Методика глубокой стимуляции мозга – применяется не повсеместно, но дает хорошие результаты. Метод заключается в ношении устройства, от которого в мозг идут электроды, стимулирующие соответствующий участок мозга.
Эффективность медикаментозного лечения оценивают по снижению симптоматики. Если консервативная терапия оказалась неэффективной, то назначают хирургическое вмешательство.
Оперативное лечение: к нему прибегают при неэффективности медикаментозного. Операция называется стереотаксической деструкцией ядер таламуса и заключается в разрушении области мозга, отвечающей за чувствительность. Процедура позволяет снизить симптоматику и вернуть способность к нормальному движению.
В клинике ЦЭЛТ работают квалифицированные неврологи, которые предлагают терапию синдрома Паркинсона. Современные методы диагностики позволяют врачам точно установить причину болезни, а многолетний опыт – назначить максимально эффективное лечение.
Кофе и болезнь Паркинсона — какая связь?
Темой недавнего исследования стало употребление кофе и болезнь Паркинсона.
Исследование показало более низкий уровень кофеина в крови у людей с болезнью Паркинсона. В исследовании сравнивали пациентов с болезнью Паркинсона, несущих определенную генетическую мутацию, которая, как известно, увеличивает риск заболевания, с другими пациентами, несущими ту же мутацию, но не имеющими данного заболевания.
Болезнь Паркинсона — это прогрессирующее заболевание головного мозга, характеризующееся тремором, ригидностью конечностей и туловища, а также проблемами с движением и равновесием. Пациенты с этим заболеванием также имеют повышенный риск депрессии и деменции.
По данным Национальной медицинской библиотеки США, более 1 миллиона человек в Северной Америке и более 4 миллионов человек во всем мире страдают болезнью Паркинсона. В США ежегодно диагноз ставится около 60 000 пациентам.
Около 15% людей с этим заболеванием имеют семейный анамнез болезни Паркинсона, что позволяет предположить, что они унаследовали гены, повышающие риск развития этого заболевания. Однако большинство случаев является результатом сложного, плохо изученного взаимодействия генетических факторов и факторов окружающей среды.
- Некоторые факторы окружающей среды, такие как травма головы, химические вещества и лекарства, связаны с повышенным риском, тогда как физические упражнения понижают этот риск.
- Обзор предыдущих исследований 2010 года показал, что чем больше люди употребляют кофеин, тем ниже у них риск развития болезни Паркинсона.
- Другое исследование показало, что у пациентов с болезнью Паркинсона, у которых нет генетических факторов риска заболевания, уровень кофеина в крови ниже, чем у людей без нее.
Группа ученых, возглавляемая исследователями из Массачусетской больницы общего профиля в Бостоне, решила выяснить, может ли кофе защитить людей с мутацией в гене LRRK2. Наличие этого гена увеличивает риск развития заболевания, но не гарантирует его.
Исследователи сравнили пациентов с болезнью Паркинсона и без нее. В обеих группах были пациенты с мутацией в гене LRRK2 и без нее.
Исследователи обнаружили, что различия в уровне кофеина в крови между пациентами с болезнью Паркинсона и без него были больше среди людей с этой генетической мутацией.
Доктор Грейс Кротти, руководившая исследованием, сообщила:
«Эти результаты являются многообещающими и стимулируют будущие исследования по изучению кофеина и методов лечения, связанных с кофеином, чтобы уменьшить вероятность того, что у людей с этим геном разовьется болезнь Паркинсона. Также возможно, что уровень кофеина в крови может быть использован в качестве биомаркера, чтобы помочь идентифицировать людей с этим геном, если уровень кофеина останется относительно стабильным».
Авторы опубликовали исследование в журнале Neurology.
Пять химических веществ, связанных с кофе
Ученые проанализировали образцы плазмы крови 368 человек, включенных в LRRK2 Cohort Consortium, исследовательский проект, учрежденный в 2009 году, который координируется и финансируется Фондом Майкла Дж. Фокса для исследований болезни Паркинсона.
В одну группу вошли 188 человек с болезнью Паркинсона, а в контрольную — 180 человек без болезни. Примерно такая же пропорция в каждой группе имела мутацию в гене LRRK2.
- Когда исследователи сравнили химический профиль плазмы двух групп, они обнаружили, что уровни пяти конкретных химических веществ различались больше всего — все они связаны с кофеином.
- Концентрации всех пяти химических веществ были значительно ниже среди людей с болезнью Паркинсона, чем у людей без этой болезни.
- Среди людей с не-мутантным геном LRRK2 концентрация кофеина была в среднем на 31% ниже в плазме у людей с болезнью Паркинсона, чем у пациентов без этой болезни.
- Уровень кофеина был на 76% ниже среди людей с болезнью Паркинсона и мутированным геном LRRK2 по сравнению с контрольной группой.
- Чтобы перепроверить свои выводы, исследователи также изучили анкеты, заполненные 212 участниками, с указанием количества потребляемого кофеина.
- Это показало, что люди с болезнью Паркинсона и мутировавшим геном LRRK2 потребляли на 41% меньше кофеина в день, чем люди, у которых не было болезни Паркинсона, независимо от того, имели они мутировавший ген или нет.
Альтернативное объяснение
Исследователи осторожно указывают на то, что их работа показала, какую связь имеет кофе с болезнью Паркинсона. Но, тем не менее, их исследование не доказало, что потребление кофеина защищает людей от этой болезни.
Например, остается вероятность того, что наличие мутации в гене LRRK2 не только увеличивает риск болезни Паркинсона у человека, но и делает его менее склонным к употреблению напитков с кофеином.
«Мы еще не знаем, склонны ли люди, предрасположенные к болезни Паркинсона, избегать употребления кофе, или почему некоторые носители мутации пьют много кофе и получают пользу от его нейропротекторного действия», — говорит профессор Кротти.
Кроме того, доктор Кротти отмечает, что в исследовании рассматривались люди в определенный момент времени, поэтому в нем ничего не говорится о том, когда возникает какой-либо защитный эффект, или как кофеин может повлиять на прогрессирование болезни. Таким образом, кофе и болезнь Паркинсона — это вопрос, на который только предстоит ответить.
Кофе уменьшил риск развития заболеваний Альцгеймера и Паркинсона
При этом эффект происходит не от кофеина, а от степени прожарки зерен.
Ученые из Исследовательского института Крембиля (Канада) изучили, как три типа кофе взаимодействуют с тау-белками и бета-амилоидами, чтобы понять, как это вещество способно бороться с причиной деменции при болезнях Паркинсона и Альцгеймера. Работа опубликована в журнале Frontiers in Neuroscience.
Ссылаясь на исследование 2011 года, авторы утверждают, что потребление кофе коррелирует со сниженным риском развития заболеваний Альцгеймера и Паркинсона. В своей работе они хотели выяснить причины такой связи.
Для этого ученые выбрали три варианта одного вида кофе (арабика): слабой обжарки, сильной обжарки и сильной обжарки без кофеина. Положительный эффект при взаимодействии с веществами, считающимися виновниками деменции, продемонстрировали две последние разновидности.
Поэтому ученые сделали вывод, что нейтрализующее воздействие оказывает не кофеин, а иной элемент, появляющийся в ходе обжарки.
Всего авторы рассматривали шесть компонентов кофе, среди которых были фенилинданы (phenylindanes) — антиоксиданты, появляющиеся только при обжаривании. Именно они, по мнению исследователей, могут предотвратить деменцию, потому что ингибируют белки бета-амилоиды и тау-белки.
Бета-амилоиды — пептиды, состоящие чаще всего из 40 аминокислотных остатков. Патогенным считается белок Aβ42, длина которого увеличивается до 42 остатков. При прогрессировании болезни Альцгеймера он накапливается и образует амилоидные бляшки.
Вместе с тем он провоцирует накопление тау-белков (нейрофибриллярных клубков). Эти клубки обнаружили у всех пациентов, страдающих от болезни Альцгеймера. При этом усиление деменции прямо коррелировало с числом клубков.
В больших количествах эти сгустки протеина начинают повреждать нейроны.
Один из исследователей доктор Росс Манчини (Ross Mancini) рассказал, как его коллеги собираются продолжить работу:
«Впервые кто-то взялся за изучение взаимодействий между фенилинданами и белками, вызывающими пагубные симптомы болезней Альцгеймера и Паркинсона. Следующий шаг — исследование того, насколько полезно это соединение и способно ли оно легко проникать в кровоток или преодолевать гематоэнцефалический барьер».
По его мнению, последнее открытие пока еще не служит однозначным свидетельством нового лекарства от перечисленных недугов. Однако если последующие исследования покажут положительные результаты, то, возможно, в будущем они приведут к созданию препаратов.
Ранее ученые из Технологического института Стивенс пришли к весьма необычным выводам: по их мнению, запах кофе способствует повышению интеллектуальных способностей, позволяя, в частности, лучше справляться с задачами по алгебре.
Как сохранить качество жизни с болезнью Паркинсона: рекомендации от экспертов столичного ИДПО
11 апреля – Всемирный день борьбы с болезнью Паркинсона. Этот недуг входит в число самых распространенных в мире хронических прогрессирующих нейродегенеративных заболеваний. По статистическим показателям он уступает пока только болезни Альцгеймера и очень часто встречается среди лиц пожилого возраста.
Но сегодня услышать подобный диагноз от врача уже не так страшно, как это было полвека назад. Люди с этим диагнозом сохраняют физическую активность, общаются с близкими и друзьями, посещают театры и выставки. Все это стало возможным за счет достижений современной медицины и учреждений социальной сферы.
За последние 20 лет доля населения старшего возраста в мире увеличилась на 48%, а еще через 10 лет этот показатель достигнет уже 56%. Пациентов с болезнью Паркинсона станет больше, ведь недуг имеет особенность молодеть и возникать у людей трудоспособного возраста: каждый десятый пациент с болезнью Паркинсона моложе 50 лет, каждый двадцатый – до 40 лет.
Как распознать предвестники
Необратимые изменения в организме запускает снижение уровня дофамина. Именно этот гормон-нейромедиатор отвечает за слаженную работу мозга и всей нервной системы. Предвестниками, или «красными флажками», болезни Паркинсона считаются нарушение обоняния, частые депрессии, расстройство пищеварения, нарушение сна, снижение активности в целом.
По мере прогрессирования заболевания могут наблюдаться скованность и замедленность движений, тремор рук, ног и головы, нарушение походки (т. н. шаркающая походка), снижение выразительности мимики, частые перемены настроения с чередующимися периодами депрессии и апатии, нарушение сна (сонливость, частые пробуждения, вскрикивания во сне), нарушение памяти.
На дальнейших этапах болезни у человека могут возникнуть проблемы с самообслуживанием. Если такому человеку не будет оказана качественная медицинская и социальная помощь, возможна полная утрата физической активности и умственных способностей вплоть до развития деменции.
«Социальный комплекс столицы располагает ресурсами для оказания помощи столкнувшимся с этим недугом, а обучение специалистов по надомному уходу и работе в специализированных учреждениях проходит на базе нашего института.
Нередко именно социальные работники первыми диагностируют признаки развивающегося заболевания у подопечных, помогают им и их близким своевременно принять меры по сдерживанию развития недуга», – говорит врач-невролог, кандидат медицинских наук, доцент ИДПО Ирина Авдеева.
Для эффективной борьбы с распространением болезни Паркинсона актуально не только ее лечение, но и профилактика, а также популяризация информации об этом недуге. Как можно больше людей должны знать, что своевременная диагностика поможет замедлить прогрессирование заболевания и сохранить качество жизни заболевших.
Как предотвратить или отсрочить болезнь Паркинсона
Прежде всего эксперты советуют повышать уровень дофамина в организме. Речь идет о правильном питании, регулярной физической активности и здоровом сне.
Для выработки дофамина необходима аминокислота тирозин, содержание которой очень велико в таких продуктах, как орехи (к примеру, грецкие, миндаль), авокадо, сезонные фрукты (бананы, клубника арбуз, яблоки), а также овсянка, семена кунжута и тыквы, фасоль, свекла, молоко, черный шоколад, зелень.
Физические нагрузки, соответствующие возрасту, стимулируют не только активность дофаминовых рецепторов, но и выработку серотонина и других эндорфинов. Занятия йогой, цигуном, долгие прогулки пешком, плавание, танцы, езда на велосипеде улучшают состояние здоровья человека, поднимают настроение, избавляют от депрессии и продлевают качественную жизнь.
Полноценный отдых помогает поддерживать необходимый уровень дофамина, дарит бодрость и ощущение удовлетворенности на целый день. Необходимо помнить: чтобы высыпаться и получать самое полезное от сна, необходимо отправляться в постель не позднее 23 часов, а в идеале между 20 и 22 часами.
Куда обращаться в случае необходимости
Каждый житель России может обратиться за диагностикой и назначением лечения в Центр болезни Паркинсона на базе Российского национального исследовательского медицинского университета имени Н. И. Пирогова Минздрава России по адресу: Москва, ул. 1-я Леонова, дом 16.
В широком доступе имеется и научно-популярная литература о заболевании, его течении и методах профилактики. Например, книга «Поговорим о болезни Паркинсона», автором которой является Джон Вайн.
Значительный прогресс наблюдается в разработке хирургических методов лечения болезни Паркинсона.
Широко применяется глубокая электростимуляция, которая имеет несомненные преимущества перед хирургическим лечением.
Семимильными шагами новые технологии лечения болезни Паркинсона развиваются благодаря достижениям фундаментальных нейронаук. Все шире внедряются экспериментальные технологии генной и клеточной терапии с использованием рекомбинантных вирусных векторов и нанолипосомальных систем доставки.
В программе Института дополнительного профессионального образования работников социальной сферы есть несколько профильных образовательных курсов: «Инструменты и порядок проведения функциональной диагностики потребностей граждан в системе долговременного ухода», «Когнитивные нарушения у людей пожилого и старческого возраста», «Практические социально-медицинские навыки по уходу на дому» и др. Пройти обучение в этих направлениях могут как социальные работники, так и сотрудники широкого спектра учреждений, работающих в сфере помощи людям с нейродегенеративными заболеваниями.
Важно понимать, что диагноз «болезнь Паркинсона» не является в современном мире приговором. Для того, чтобы не дрогнуть перед таким серьезным испытанием в жизни, важны три фактора: качественное лечение, своевременная профилактика и диагностика, а также желание самого человека активно заниматься собой и своим здоровьем.
Источник